突破海外专利壁垒,艾博生物成功研发出基于Cis系统的环状RNA
苏州2024年8月22日 /美通社/ -- 2024年8月21日,艾博生物于Nucleic Acids Research发表论文"Efficient circularization of protein-encoding RNAs via a novel cis-splicing system",报道了其自主研发的高效RNA成环顺式剪接系统(下称"Cis系统")。该系统制备的环状RNA (circRNA)能大幅延长蛋白表达、降低天然免疫激活,并具有剪接位点设计灵活性等优势,拥有广阔的应用潜力。

已发表论文截图
近年来,环状RNA技术在生物医药产业界备受瞩目,已有多家工程化环状RNA公司创立,这些公司筹集了超过10亿美元的融资。其中最受关注的当属Flagship孵化的Sail Biomedicines(由Laronde, Senda Biosciences合并而成),已累计融资近8亿美元,而麻省理工学院(MIT)Daniel Anderson教授创立的Orna Therapeutics 在获得超3亿美元融资后,今年又宣布收购ReNAgade Therapeutics,进一步加速其临床产品的开发。
艾博生物凭借其业界领先的mRNA和纳米递送技术平台,在不断发展的过程中累积了丰富的研发经验,成功开发出全新的环状RNA技术平台,展现了艾博生物在核酸药物开发领域强大的研发实力与创新能力。
艾博生物全新的环状RNA系统拥有全球自主知识产权,突破海外公司PIE系统专利限制
目前应用较多的体外合成circ RNA技术是PIE法(Permuted Introns and Exons),代表公司如Orna Therapeutics已对PIE系统申请专利保护,该技术的核心优化工作由MIT相关专家完成,并在多个国家和地区进行了专利布局。
本论文介绍的Cis系统的环状RNA PCT专利已进入公开审评阶段,该系统突破了海外公司PIE系统底层专利的限制,特别适合于环状RNA药物的开发和工业应用。如论文所报道,艾博生物研发的Cis系统通过在前体RNA的一端嵌入核酶核心结构,消除了在核酶和目标基因间需额外引入间隔元件的必要性,简化了环化步骤并提升了效率,从而具备"无痕"、高效翻译的优点,也克服了高效合成高质量circRNA等技术难题。
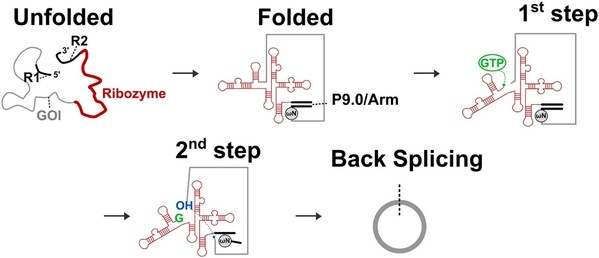
含核酶的前体RNA通过连续两步顺式自剪接反应实现目标序列首尾连接环化
基于Cis系统的环状RNA拥有广阔前景,未来可期
本研究报道的Cis系统环化效率高,并且对RNA分子两端的碱基和序列组成基本无限制,能够真正做到高效且无痕的环化。此外,Cis系统设计更简单灵活,可根据特定治疗需求定制化设计,兼容不同长度的RNA分子,最终可以实现更加持久的蛋白表达,低天然免疫刺激,及潜在组织特异性表达,在蛋白替代等慢性疾病治疗及免疫治疗领域,或需重复给药的治疗策略方面展现出卓越的应用前景。基于这些优势,新型Cis系统有望成为高效制备高质量环状RNA的突破性技术,更好的赋能环状RNA药物在传染病及肿瘤疫苗,细胞及基因治疗等领域核酸药物的开发。
艾博生物mRNA创新高级研究员杞少鋆博士(核酸科学部门)表示:
"我深切感受到,公司所提供的优越科研条件和创新氛围是我们成功突破环状RNA技术关键瓶颈的重要基石。在这里,每一次技术进步和创新成果的诞生,都是公司对研发持续投入的结果。"
艾博生物副总裁郜鹏博士(亦是本论文通讯作者)表示:
"经过两年多的攻坚,我们团队最终突破了环状RNA技术的关键瓶颈。目前,相关应用研究已经取得了初步成果,证明了该技术的潜在价值与可行性。我们希望尽快将这一原创性成果转化为实用的解决方案,推动医学研究与产业的进步。"
原文链接:
Shaojun Qi, Huiming Wang, Guopeng Liu, Qianshan Qin, Peng Gao, Bo Ying, Efficient circularization of protein-encoding RNAs via a novel cis-splicing system, Nucleic Acids Research, 2024;, gkae711, https://doi.org/10.1093/nar/gkae711